Какво е луминол луминол как да се направи у дома
Някои вещества, които участват в химични реакции, имат способността да излъчват светлина. Всеки любител химик веднъж произведени блестящия течността. В тази статия ще се обсъждат, че е луминол, как да се готви у дома.
Какво е хемилуминесценция?
Много реакции в химията възникнат с освобождаването на енергия. В повечето експерименти, енергията се освобождава под формата на топлина. В реакцията на алкални и кисели разтвори се нагрява. Има случаи, когато енергията може да се прояви под формата на електрически ток (експерименти с електрохимични клетки). В енергията горене на реагентите се превръща в топлина и светлина.
Но има и реакции при които се провежда светлинно излъчване,, но няма повишаване на температурата. Това явление се нарича хемилуминесценция. Най-ярък пример - студена фосфор сияние. Трябва да се отбележи, че в повечето химични реакции освобождават "студена светлина" органични съединения се окисляват. Оксиданти обикновено действат кислород или водороден прекис.
В природата има много вещества, които могат да излъчват светлина. Но повечето от светлината, получена е много слаб и може да се открие само със специално оборудване.
Към светло и красив хемилуминисценцията в състояние на относително малка група от органични и неорганични съединения. В примерите следните материали: луминолни, силокси, lofin и lyutsegenin difeniloksalat.

Какво е луминол?
Луминол се синтезира в Германия през 1902 г., но истинското му име е по-късно. Това е бяло кристално или светложълт цвят, лесно разтворими в полярни органични разтворители. Във водата, луминол е напълно неразтворим.
Тази органична материя е способна да освобождава светлина, когато се комбинира с водороден прекис или други оксиданти. В неутрални и слабо кисели течности, под ултравиолетова светлина, то флуоресцира светлосиня светлина. В алкални разтвори (водороден пероксид), където реакцията протича в присъствието на катализатори - фосфорно съединение, метални соли на хемин и хемоглобин - луминисценция, получени по-наситени и ярки.
Процесът се състои от два етапа. Киселина се загрява с хидразин в органичен разтворител с висока точка на кипене (3-етилен гликол). Кондензацията на хетероцикличната система се получава 5-nitroftalilgidrazida. Това съединение се редуцира с помощта на амониев сулфид и получената образува луминол. Ръцете това могат да бъдат получени в лаборатория синтеза на 3-нитро-фталова киселина.

Когато използването на луминол
Въпросното вещество е забележителни реагира с желязото, което е част от хемоглобина. Ето защо, тя се използва широко в експерти по съдебна медицина в идентифицирането на кръвни следи и пръстови отпечатъци, оставени на местопрестъплението. Луминол се използва учени по време на различни биологични изследвания за откриване на желязо, мед и цианид.
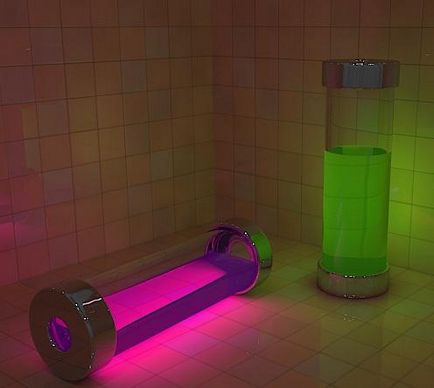
Къде да купя луминол разтвор
луминол цена е доста висока. Възможно е да се погледне химични форуми, специални бази или в аптеките. Ако не знаете откъде да вземе луминол, можете да закупите в аптеката "Galavit", която е на разположение в таблетки, капсули и свещички. Една таблетка съдържа 25 мг натриева сол на луминол. Към 50 мл 1% разтвор трябва да е 20 таблетки (опаковане). Таблетките се смилат на прах и след това се добавя вода към него.

Светлинният течност водороден прекис
Има рецепти за светеща течност импровизирани. Но за решение най-добре използвани луминол, защото това дава гладка и мека синкава светлина. Преди да започнете, не забравяйте да защитят откритите части на плътна тъкан на тялото, и на ръцете, носете ръкавици.
Подгответе луминол у дома си в класическата (първи) рецепта:
- Луминол - 2-3 грама.
- Вода - 0.1 литра.
- Разтвор на водороден пероксид (3%), - 0.08 литра.
- Сода каустик - 0.01 литра.
- Bluestone - 3 грама.
- Оцветители (рубли, блестящ зелен или който и да е друг).
- Стъклени (колби или буркани).
- Излива се в стъклен контейнер и добавяне на вода луминол. Разбъркайте добре кристалите във вода, така че те се максимизира разтваря.
- Към получения разтвор се прибавя водороден прекис.
- Полученият състав добавяне на меден сулфат. Може замени сулфат хлорид или железен сол кръв.
- Най-новата композиция да прикачите сода каустик.
- В стаята се изключи светлината. Полученият състав трябва да излъчват светло синя светлина. Ако различен цвят, след това добавяне към разтвора на подходяща флуоресцентно багрило.
- разтвор луминол (3%) - 5 мл.
- Gidroperit (3%) - 10 мл.
- Пране с вода - 20 мл.
- калиев перманганат.
- Всеки стъклен буркан или пот.
- Контейнерът се изсипва луминолни разтвори, препарат на прах и водороден пероксид.
- Внимателно разтривайте няколко кристала калиев перманганат и се добавя към общия състав.
- За да видите това, което луминол и как тя ще се прояви неговите свойства, изключете светлината в стаята. Течността ще издаде красив блясък. Ако разтворът се разбърква периодично, пенливи пяната се появява на повърхността им.

Приготвяне на разтвора с диметил сулфоксид
По-интересно изпълнение ще луминол окисляване с атмосферен кислород в Dimexidum среда. Луминисценцията се извършва в интерфейса на раздел замърсяването на въздуха и вода.
ние трябва да се подготви състава:
- Луминол - 0,15 грама.
- Dimexidum (DMSO) - 30 мл.
- Суха луга - 35 грама.
- Всяко флуоресцентно багрило.
- Висока стъклария.
- Основно смесват в колба dimexide, луминол и алкали.
- Съдът се затваря плътно с капак.
- В стаята се изключи светлината.
- Колбата се разклати леко да се получи синкаво сияние. За промяна на цвета на добавяне на флуоресцентно багрило.
- Ако светлината е загубила своя блясък, е възможно да се отвори контейнера. На влизане на въздух в колба, отново става ярко разтвор и наситен.
Готварство Съвети
Много алкален в разтвора не се препоръчва да се добави, тъй като това е много трудно да се разтвори и се превръща течността в гъста каша. Суспензията на луминол Dimexidum и алкален може да се съхранява за дълъг период от време. При добавяне на окислител сияние ще бъде еднаква. Продължителността му зависи от броя и gidroperita луминол и може да достигне до 40 минути. Но от изобилие на луминол светлина се превръща в по-слаба.
Трябва да се отбележи, че яркостта на луминесценция и продължителността ще зависи и концентрация луминол. Силно разредени разтвори дават слаб, но дълго сияние. Голяма концентрация на материал образува силен яркост на целия разтвор. Цвят на светлината може да варира от синьо до зелено. В богатите състави, съдържащи по-голяма концентрация на кръвни соли получени зелена светлина.

Възможно ли е да се замени луминол?
Има ситуации, когато е необходимо да се подготви светлинен течност без луминол. За да направите това, вземете борна киселина и няколко капки флуоресцеин. Тези вещества се изисква да се смесват и се загрява метална плоча. Liquid ще светят в тъмното за около минута.
За да се разбере това, което е луминол, по-добре се опитайте да го получите себе си. Както се казва, по-добре да се види веднъж от чуят стотици пъти. Но не забравяйте, че всички опити включват взаимодействие с корозивни и вредни вещества. Поради това е необходимо да се спазват мерките за безопасност.
