Практическа работа - производството на водород в лаборатория и учи неговите свойства
урок Местоположение: 8-ми клас. Предмет II: кислород, водород, вода като разтворител.
Вид на урока. практическа работа
- Образование - разработване на експериментални умения - техники за работа с лабораторно оборудване и материали; способността да се спазват, се правят изводи, да види резултатите от практическата работа в тетрадка.
- Развитие - работа върху развитието на умения умелото боравене с огън, опасни вещества.
- Образователно - разширяване на хоризонтите на учениците, формиране на уважение към историята на науката.
- здраве училище - разработване на идеи за здравословен начин на живот в блоковете: "Химия в ежедневието - безопасно поведение"
Очаквани резултати от обучението:
- Бъдете в състояние да работят с автоматично устройство за газ Kiryushkina
- За да може да се съберат на газа от водоизместимост
- За да може да се проверява чистотата на горивния газ
- За да може да се направи правилните изводи от наблюдаваните експерименти и да се характеризира свойствата на водород
- Мултимедийна презентация 2 (Microsoft Power Point)
- Гащеризони - хавлия
- Заетостта на лабораторно тава зеница (13 бр.)
- Лабораторни статив стъпалото, тест държач тръба рейка епруветка, лъжица опаковка, филтърна хартия
- алкохол печка, мачове
- Kiryushkina автоматично устройство за газови тръби 3, матрицата с вода
- Цинк гранули, солна киселина (разредена.), Меден оксид (II)
- Заетост на лаборатория тава за учителя:
- за тавата за студент
- Крусибъл клещи, стъкло, плоско стъкло, стъклена пръчка
- "Резултати" нарушения на правилата за безопасност
(В курсив описва действията на студентите и преподавателите, особено техники урок нормален шрифт - реч на учителя)
I. организационния точка (1 мин.)
имайте предвид наличието на рокли за всички ученици, безплатно да проверят дали торбичките с пасажи, ако влакната на момичета отстранени. На масите оставят само химикалки, калкулатори и преносими компютри.
II. Активирането на знанията, необходими за осъществяване на практическата работа (13 мин.)

В този урок, ние получаваме водород в лабораторията. Това газообразно вещество; Тя е взривоопасен, ако въздухът е замърсен, и следователно изисква по-голямо внимание.
Учениците в същото време с обсъждането боядисани в дневника за безопасност.

В предишния урок, учениците бяха обучени на тази практическа работа (Slide 1) и предвид домашното:

Slide проявява постепенно, в съответствие с разговора

- Какви са изходните материали, ние ще използваме за производството на водород?
- Необходимо ли е да се загрее реакционната смес?
- Какво да търсите при спазване на записа?
- Кое устройство ще се използва за производството на водород?
- Какви са някои начини да се събират водород, защо?
Slide проявява постепенно, в съответствие с разговора

- Как да се докаже наличието на водород в тръба-приемник?
- Какво се осъществява химична реакция в същото време?
- Какво да търсите при запис на наблюдения в този раздел на работа?
- Какво е най-детониращи газ?
Ако възникне експлозия в стъклен съд, тези части могат да наранят другите и експериментатор.
При тестването на чистотата на водород се изгаря малък обем (около 15 мл).
Възможно нараняване микро експлозия не може да води.
Член TB: Не смятам, че газа, отделян от устройството чист, дръжте отваряне тръба пари далеч от пламък дух лампа.
Демонстрация на безопасност правила резултати Нарушение: епруветка с напукана дъно

Член TB. нагряване на тръбата трябва да бъде на мястото, където твърдата фаза, а не по-горе -, където въздухът. Чрез неравномерно загряване на тръбата ще се счупи.
тръба със следи от солна киселина в смес с меден оксид (II)
Член TB: автоматичното устройство на солна киселина зареждане необходимо да се внимава да не се изсипва киселина (макс 2 мл), в противен случай излишъкът от екзотермичният процес на процеса и бързо спада в тръбата за пара.
III. експеримент Демонстрация учител (7 мин.)
Учителят по дума с разговорни елементи

1. Mark лъжица дозиране малко количество черен прах на меден оксид (II), който се поставя в епруветка, се оставя да престои за епруветки за провеждане на експерименти върху свойствата на възстановяване водород.
2. Фиксирайте автоматичен инструмент за газ в триножник крак. Зареждащи прекурсори единица: 4-5 цинк гранули пуснати в гумена кръг фуния пренапрежение солна киселина така, че слой от цинк не е повече от 2 мл. Устройството е затворен херметически като е възможно.
3. За проверка на чистотата на газа, трябва да се подготви лампата алкохол в аванс. Можете да работят заедно и да запали лампата дух след газ ще получат в probirku- приемник.
Правила TB: работа с дух-лампа
а) преди да светне лампата на алкохол, трябва да се провери дали диска е здраво до пристанището на резервоара (в противен случай искрата може да попадне в резервоара и целия обем на алкохола ще изгори)
б) само един мач на светлина (не използвайте по-лека, друг дух-лампа)
в) на мача трябва да се постави в тавата, като се уверите, че е погасено (демонстрация на безопасността правила нарушение - закалени тава)
ж) да гасят пламъците, тя трябва да се затвори капачката (взриви невъзможно)
Съберете зараждащата водород въздушен обем тръба стопанство приемник с главата надолу. Проверка за газ чистота: фиксиращ палец дупка тръби и да доведе до алкохол лампа пламък тръба, да го отворите.
4. След сглобяване зараждащата водород, чрез изместване на вода: набиране тръба пълна с вода, да го превърне в матрицата и да доведе до контакт пара тръба. Когато тръбата за приемник е изцяло запълнена с водород, фиксиращ палец отваряне вода. Уверете чистота газ.
5. определи епруветката с меден оксид (II) в държача.
Правила TB: фиксиране на тръбите в държач
а) на тръбата е фиксирана в горната трета част близо до отвора
б) тръба не трябва да пада, но се върти (в противен случай при нагряване се разширява и стъклена тръба може да се спука)
в) за отстраняване на тръбата от титуляра, трябва да се разхлабят скобата.
Загрява се флакон пламък дух лампата 2-3 пъти повече се загрява в горната част на пламъка, на мястото, където има меден оксид (II). Направи тръба пара да се освободи водород.
След края на експеримента в епруветката да се охлади, след това се поставя в шкаф за епруветки.
6. гасят алкохол лампа, освобождаване скоба блок на водород.
Основното правило на TB: сигурни ръце, за да работят!
IV. Извършване практическа работа, представяне на резултатите, почистване на работното място (23 мин.)
1. Студентите изпълняват практическа работа самостоятелно. Учителят следи за правилното-ност изпълнява експериментални техники и спазване на правилата за безопасност.
2. Почистване на работното място: след края на експеримента за изследване свойства за намаляване на водород:
Първият студент: да гасят дух лампата, даде тръба-реактора, за да се охлади, след което го поставя в шкаф за епруветки.
Второ студент: блокира освобождаването на газ в устройството за автоматично, премахване на фунията, цинкови остатъци поставят върху филтърна хартия. Извадете инструмента от краката на триногата, се налива отрова-бот решение в "Флакон от да се оттече", мине учителя табло.
Учител: събиране на тави и форми с вода.
3. Демонстрация опит: изследване на реакционният продукт на цинк със солна kiclotoy

Отработеното разтвор се оттича в бехерова чаша и няколко капки със стъклена пръчка за прехвърляне към стъклена пластина. Засилване плоча в тигела клещите и изпаряване на разтвора в продължение на пламък
4. Проверка на резултатите от експеримента: да формулира и напишете наблюдения, заключението (това научих от водород в газообразно състояние в практическа работа), за да предадат на ноутбука.
Използвани електронни помощни средства:
Осъществяване работа в тетрадки ученик:
Практическа работа 5: Производство на водород и изследване на неговите свойства
1. Метод за производство на водород - взаимодействието на активните метали с киселини.
Zn + 2HCl = ZnCl2 + Н2 ↑ + Q - при нормални условия
- Реакционната между цинкови гранули със солна киселина бавно в началото, след това много бързо, тръбата се нагрява
- пара, освободена от тръбите безцветно газове
- чрез изпаряване на получения разтвор е бял прах върху стъклена плоча
2. Устройство за получаване и събиране на водород

Фиг. Устройство за водород - автоматично, което позволява по всяко време, за да се спре реакцията със скоба (Kiryushkina устройство).
Бране на газа от водоизместимост - може би, защото водород слабо разтворим в него.

Фиг. Събиране на газ по въздух изместване - държите тубата приемник с главата надолу, защото
- следователно, по-лек от въздуха, водород
3. Откриване на водород - да се провери неговата чистота

- чрез изгаряне на първа част от газа се разпространява остър лай звук
- по време на горенето на втората част газ се чува лек памук Фигура 5 "р-слабините"
4. водород имот - активно редуктор
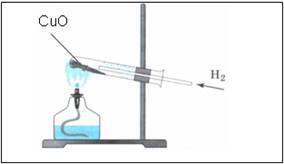
- прах променя цвета от черно към мед
- по стените на тръбите се появяват безцветни течни капчици
Един метод за производство на водород в лабораторията е реакцията на цинк с разредена. солна киселина и образуваната сол (цинков хлорид) и водород. Водород - газ безцветен, без мирис, слабо разтворим във вода, по-лек от въздуха, се смесва с въздуха експлозивни възстановява метали от техните оксиди.