08 - Получаване на разтворите и определяне концентрацията им (NP)
Получаване на разтвор точната концентрация на
(Титрува със стандартен разтвор).
Титратния се приготвя по различни начини.
1. Ако вземем точно проба от желания вещество (т, г) да го прехвърля количествено в мерителна колба (V, мл), разтваря се и се пълни с дестилирана вода до марката, и след това затваряне на запушалката и се разбърква, получаваме желаната концентрация на разтвор с известен титър T =
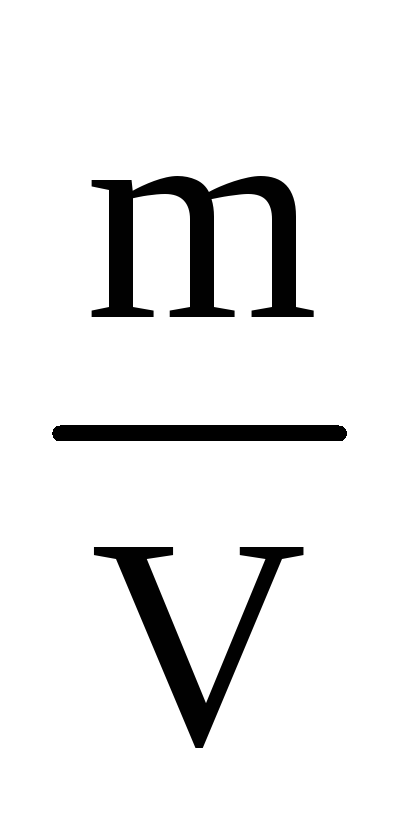
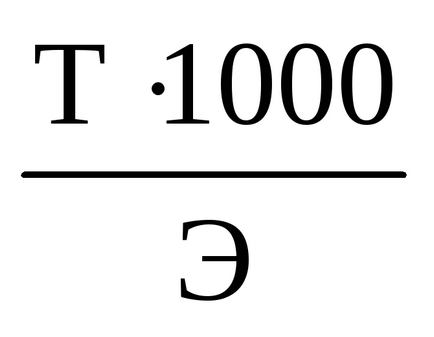
2. титратния се получава и с помощта на "fiksanaly" - стандартни-заглавия. Те са запечатани стъклена ампула, съдържаща точно претеглени количества от различни кристални вещества или точно отмерени количества титрант необходимо за получаване на 1 литър разтвор нормалност точно известни, например 0.1 N (най-често), 0.05 N, и т.н.
Както Шишето се запечатва, след fiksanal може да се съхранява дълго време, с изключение на основи, които са на склад бързо стана мътен поради взаимодействието на ампули алкални стъкло. Изхвърли облачност разтвори трябва да се използват не са подходящи.
Получаване на титрант стандарт титър се редуцира до прехвърля количествено към съдържанието на ампулата в мерителна колба с капацитет 1 литър, и след това се разтваря вещество и полученият разтвор се разрежда до марката с дестилирана вода.
Стандартните методи за прехвърляне на колба титър.
За прехвърляне материал в мерителна колба врата 1литър фуния, поставена в предотвратяване на ударника, за които определят fiksanala флакон тънък вдлъбнатина дъно. Леко въздействие върху ампулата насрещната прекъсне стъклото и счупване на остър тръстика горния отвор във флакона, веществото се прехвърля в мерителна колба. Чрез отвора старателно се промива с дестилирана вода съдържание ампула, фуния и се промива чрез отстраняване, обемът на разтвора се регулира в колбата до марката с дестилирана вода.
стъклена фуния добавя мерителна колба. От едната страна на ампулата с перфоратор щифт. Provernuv флакон, напълно го освободи от съдържанието и старателно се промива с дестилирана вода от вътрешната страна в размер на шест пъти обема на ампулата. Разтворете съдържанието на флакона в колбата, донесе обем на течността до маркировката и разбъркайте добре.
ВНИМАНИЕ. Ампула стандарт титър фуния, стъкло ударник, трябва да бъде старателно се промива с вода, с етикет ампула трябва да се отстрани.
Начин на приготвяне разтвор с
Получаване на предварително определена концентрация на концентрирания разтвор чрез разреждане с вода, като се използва хидрометър (денсиметър)
Предварително определена плътност на концентрирания разтвор с хидрометър.
Хидрометър е кух термично затворен съд с приложена върху него етикети (обикновено прикрепени към мащаб стена хартия деленията вътрешни). В долната част на стоки, поставени (фракция), при което хидрометър потопени в течността, поддържан в изправено положение.
Концентрираният разтвор се излива в цилиндъра, така че да не се случи чрез преливане на кръв чрез потапяне област хидрометър и хидрометър да не докосва дъното на цилиндъра. Хидрометър трябва да е чиста и суха. През отчетния ареометърът не трябва да се върти и да се докоснат до стените на цилиндъра. По скала хидрометър четения го казват с определена точност. Разделянето на скалата, която съвпада с нивото на течността показва плътността на разтвора. Вдигане на хидрометър 1-2 см, отново потопени в разтвора и за пореден път да вземе показания.
При използване на хидрометър трябва да се забравя, че температурата на разтвора трябва да съответства на температурата, при която се калибрира.
Определяне на плътността на концентрирания разтвор, в съответствие с таблицата "масова фракция и плътност на разтвора" намерено масова част на веществото в разтвора и след това изчисление се извършва. Определя се обемът на концентриран разтвор, който трябва да се вземат за да се получи разтвор с определена концентрация и предварително определен обем.
При липса на стойност плътност Таблица намерени хидрометър, неговата съответна маса фракция на вещество (концентрация процента) се определя чрез интерполация - междинна стойност за определяне две крайни. За да направите това, да направите необходимите изчисления.
Например, към разтвор на KNO3 плътност 0,0183 липсва, но има и други стойности 1,076 и 1,090. Те съответстват на концентрация от 12% и 14%.
Намери разлика от плътности и концентрации:
Полученият броя добавен в по-малка стойност, взети от таблицата концентрацията на 12 + 1 = 13% - е концентрацията на разтвора за изпитване.
Приготвяне на разтвора на кристално твърдо вещество и вода.
Да предположим, че е необходимо за получаване на 250 мл от 0.1 N разтвор на NaOH (Мае = 40 г / мол). Тъй като хидроксиди на алкални метали карбонати съдържат примеси, влага и други вещества, за да се получи разтвор точно определена концентрация на кристален алкални и вода е невъзможно. Следователно подготви суров разтвор (с концентрация близо до целта) и изясняване на неговата концентрация титруване разтвор с точно известна концентрация.
Методи за получаване на разтвора
пробата на алкален необходимата изчислява за готвене предварително определено разтвор: m = N · V · Мае = 0,1 0.25 · 40 = 1гр
Претеглят изчисленото количество алкален в химико-технически везна с точност до 0.01 грам теглене е в внимателно се промива и се суши филтърна хартия порцелан чаша или стъкло, масата на която е предварително определена.
Алкално избран шпатула или пластмасови пинсети.
Полученият претегля в ерленмайерова колба, измерване изисква цилиндър количество вода (обем разтвор за грубо вода може да се приема равен на обема на разтвора) неколкократно изплакване порцелан (стъкло) чаша и се изсипва вода в колбата с алкали. Разтварянето на алкален тел първо в малко количество вода при енергично разбъркване, поне алкален разтваряне добавят следните части вода. След процедурата, разтворът трябва да се размеси добре.
Определяне на точната концентрация на разтвора на алкален титруване със солна киселина
Pure изплакване бюрета малко количество от получава алкален разтвор. Засилване бюрета скоба в държача и го напълни през фуния с разтвор на NaOH (или КОН) до нула (на дъното на границата на менискус). Уверете се, че върхът на бюрета се изпълни с решения. Сложете на статив щанд бял лист. Аспирирайте внимателно пипетира в конична колба, 10 мл солна киселина титрант, се добавят 1-2 капки индикатор фенолфталеин и се титрува. Разтворът на алкален се добавя на малки порции, докато разтворът се разбърква в кръгово движение в конична колба. След неутрализиране на всички киселината, произтичащи от уравнението:
HCl + NaOH = NaCl + H2O
добавяне на допълнително капка разтвор на алкална ще доведе до появата на розов цвят. Титруване се счита за приключена, когато розовият цвят на разтвора изчезва в колбата при разбъркване в продължение на 30 секунди. Брой бюрета обем на база, необходима да неутрализира киселината. Титруване прекарват най-малко три пъти. всеки път от нулата. Обемите на прекарал луга не трябва да се различават с повече от 0,1-0,2 мл. От тези резултати, да вземе средната стойност и се изчислява точната концентрация на алкален с формулата:
Лабораторни упражнения
Приготвя fiksanala на 0.1N солна киселина - Стандартен разтвор.
Получава се разтвор на NaOH (или КОН) с приблизителна концентрация в плоскодънна колба на индивидуална задача.
Определя се плътността на хидрометър алкален разтвор, и се изчислява нормална концентрация.
Определете точната концентрация разтвор на алкален титруване със стандартен разтвор на солна киселина.
Сравнете резултатите, получени в претенциите. 3 и 4.
Подреждане лаборатория регистър, в резултат на изчисленията за всяка секция и кратко описание на операциите.