урок 29
В Урок 29 "Концепцията на основание" Разбира се "Химия за манекени", ще се запознаете с нов клас химикали - бази, а също и да научат за нов тип химически реакции - обменни реакции.

Както вече знаем, взаимодействието на активните метали и техните оксиди са оформени с водна основа - съединения, които не принадлежат към някоя от известните неподвижни класове оксиди, соли или киселини.
Основи като комплексни вещества
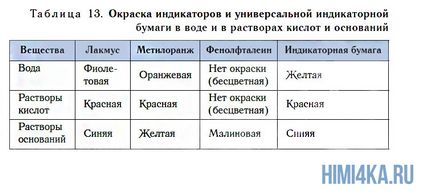
Ние тествахме използване на индикаторния разтвор получен чрез взаимодействие на СаО на калциев оксид с вода. Към това добавете към него 1-2 капки метил оранжев разтвор. цвят на разтвора се променя от оранжев до жълт (фиг. 111).

Това показва, че в това решение не е киселина, както и някои нови материали, промяна на цвета на индикатора. Като калциев оксид реагира с вода и някои други оксиди като натриев оксид Na2 О:
Реакцията на калциев оксид и натриев с вода образува вещество Са (ОН) 2 и NaOH. Те са подобни с това, че те съдържат метални атоми, и ОН група. gidroksogrupp се наричат (от гръцката дума "Hydor", което означава "вода"). Тези вещества принадлежат към класа на бази.
Основания - комплексни вещества, състоящи се от метални атоми и gidroksogrupp.
единство Валенцията gidroksogrupp. Знаейки това, че е лесно да се направи всяка основа формула: брой на ОН-групи в база формулата е винаги равно на валентността на металния атом. например:
В същото време база съгласно формулата може лесно да определи валентността на металните атоми, съдържащи се в него - той присъства във формула chislugidroksogrupp база. Например, основа във формула Fe (ОН) 2 два gidroksogrupp следователно валентността на железни атоми в това съединение е II, и в основата на хром (ОН) 3 е равно на валентността на хром атоми III.
Както е добре известно като база? Известно е, че продукти на съединенията с вода вещества се наричат хидрати. Ако вода свързан метални оксиди са оформени хидравличен Ата и метален оксид. или съкращение метални хидроксиди. Следователно, средството Са (ОН) 2 и NaOH, образуван от взаимодействието на калциев и натриев оксид с вода, наречен "калциев хидроксид" и "натриев хидроксид".
Чрез вода разтворимост съображения са разделени на разтворими и неразтворими. бази разтворими във вода се нарича основи. Те включват КОН, NaOH, Са (ОН) 2. Ва (ОН) 2 и др.
Открие присъствието на разтворим база вода (алкален) може да бъде на промяна на цвета индикатор. Освен известния лакмус метилово оранжево, а за тези цели, можете да използвате друг показател - фенолфталеин. Той няма цвят във водата и в кисел разтвор, но в присъствието на основа, този показател е оцветен в цвят магента (вж. Фиг. 111, пл. 13).
Реакционната неутрализация
Както е показано, водоразтворими бази - основи - лесно открити от показатели. Въпреки това, ако разтвор на натриев хидроксид, натриев хидроксид се добави фенолфталеин и след това солна киселина, първото червено оцветяване се появи след добавяне на киселина изчезва (фиг. 112).

Това показва, че като киселина ще унищожи или неутрализира базата. Реакцията между киселината и основата протичащ в този случай се нарича реакция неутрализация:
неутрализация реакция - реакция между основата и киселината, в резултат на образуваната сол и водата.
Реакционната неутрализация не принадлежи към някое от известните видове неподвижни реакции (заместени разграждане). Това е реакцията на нов тип - обменна реакция.
Exchange реакции са наречени реакции между сложни вещества, в които те обменят техните съставни части.
Основата се състои от метални атоми и gidroksogrupp и киселина - водороден атом или киселинен остатък. Взаимодействието на изходните материали обменя техните съставни части (фигура 113.):
Кратки изводи урок:
- Основания - комплексни вещества, състоящи се от метални атоми и gidroksogrupp.
- Реакцията между киселина и основа, при което образуваната сол и водата, наречена неутрализиране на реакцията.
- Метатеза - реакция между сложни вещества, в резултат на което те комуникират с техните съставни части.