Атомна водород - знаете как
Атомна водород. Ако разтвор на железен хлорид FeCl3 прибавя солна киселина и се хвърля в парче цинков разтвор, зараждащата водород бързо се превръща в железен хлорид FeCl2. както може да се види на прехода на разтвора в жълт цвят зелен присъщ железен хлорид:
Когато разтвор на FeCl3 се пропуска през водороден газ, например газомер, тази реакция не се появява. Може да се предположи, че специфичната активност, проявявай от водород в този случай, поради факта, че водород реагира с железен хлорид "по време на изолиране" на химическо съединение, когато неговите атоми не са били в състояние да се свърже с молекула.
Това предположение направени в миналия век, беше потвърдено косвено условие, че когато в свободно състояние т.нар атомен водород, т. Е. водород състои не от Н2 молекули. и от отделните атоми и разгледа неговата реактивност.
При високи температури, молекулите водородните атоми се разпадат в:
Атомна водород могат да бъдат получени чрез действието на безшумен електрически разряд в обикновен водород под налягане от около 0.5 mm. Създадена в тези условия, водородните атоми не са пряко свързани обратно към молекулите, което дава възможност да се изследват техните химични свойства. Атомна водород дори при обикновени температури възстановява много метални оксиди е пряко свързани с сяра, азот и фосфор; с кислород, образува водороден пероксид.
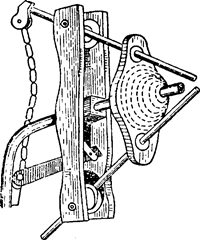
Фиг. 59. Горелка за атомен водород
При разлагане на водородни атоми абсорбира в голямо количество топлина, е 105 ккал на 1 grammolekulu:
Следователно, това означава, че водородните атоми трябва да бъде много по-активен от молекулата си. За обикновен водород влезе в реакция, първо трябва да се разтвори в молекули атома, които е необходимо да се изразходва голямо количество енергия. По време на реакциите са необходими водородните атоми на тези енергийни разходи.
Загрява се изразходва за разлагането на водородни молекули в атоми, означава, когато тези атоми са свързани в молекулата.
Този принцип се основава горелки устройства атомен водород (фиг. 59). Поток от водород от контейнера преминава през електрическа дъга, образувана между два волфрамови електроди. В този случай водородни молекули се разделят на атоми, които са свързани отново в молекулата на малко разстояние от дъгата, образувайки много горещ пламък. Високата температура на пламъка се причинява в този случай не е водород горене, и образуването на неговите молекулни атома. Този процес протича най-бързо на повърхността на различни метали, които по този начин може да се нагрява до температура над 4000 °. В атомно водород лесно стопи всички метали. и най-огнеупорния материал от тях -volfram (темп. пл. 3380 °). Тъй атомен водород, освен това, той има силно намаляване на способността, пламъкът е особено подходящ за заваряване на метали податливи на окисление.